การพัฒนาแบตเตอรี่นาไอออนแบบกึ่งโซลิดสเตตโดยใช้แคโทดสีน้ำเงินปรัสเซียนที่มีน้ำน้อยที่สุด
หวัง คุนเผิง ,1, หลิว จ้าวหลิน2, หลิน ชุนเซิง2, หวัง จือหยู ,1,2
1. ห้องปฏิบัติการหลักของ State Key of Fine Chemicals, School of Chemical Engineering, Dalian University of Technology, Dalian 116024, China
2. สาขาการพัฒนาวัสดุใหม่ Valiant Co., Ltd., Yantai 265503, China
เชิงนามธรรม
เมื่อเปรียบเทียบกับแบตเตอรี่ Li-ion แบตเตอรี่ Na-ion ให้ข้อดีด้านต้นทุนที่ต่ำ ประสิทธิภาพการทำงานที่อุณหภูมิต่ำที่ดี และความปลอดภัย ซึ่งดึงดูดความสนใจอย่างมากในการใช้งานที่คำนึงถึงต้นทุนและความน่าเชื่อถือ ด้วยความจุสูงและต้นทุนต่ำ วัสดุคล้ายสีน้ำเงินปรัสเซียน (PBA) จึงถือเป็นวัสดุแคโทดที่มีแนวโน้มสำหรับแบตเตอรี่ Na-ion อย่างไรก็ตาม การมีอยู่ของน้ำที่เป็นผลึกภายในโครงสร้างทำให้ประสิทธิภาพการทำงานของแบตเตอรี่ลดลงอย่างรวดเร็ว ซึ่งทำหน้าที่เป็นคอขวดที่สำคัญซึ่งจำกัดการใช้งาน งานนี้รายงานกลยุทธ์การบำบัดด้วยความร้อนอย่างง่ายดายเพื่อกำจัดน้ำที่เป็นผลึกออกจากวัสดุแคโทด PBAs ได้อย่างมีประสิทธิภาพ โดยปรับปรุงการรักษากำลังการผลิตจาก 73% เป็น 88% หลังจาก 340 รอบ การวิเคราะห์ในแหล่งกำเนิดเผยให้เห็นว่าการสูญเสียประสิทธิภาพคูลอมบิกของแคโทด PBA ในขั้นต้นนั้นเป็นผลมาจากการเปลี่ยนแปลงที่ไม่สามารถย้อนกลับจากรูปแบบตรีโกณมิติไปเป็นเฟสลูกบาศก์ในระหว่างกระบวนการชาร์จและการคายประจุ ปัญหานี้สามารถแก้ไขได้ด้วยการใช้ Na2C2O4 เพื่อชดเชยการสูญเสีย Na ในแคโทดที่ไม่สามารถกลับคืนสภาพเดิมได้ บนพื้นฐานนี้ แบตเตอรี่ Na-ion กึ่งโซลิดสเตตประสิทธิภาพสูงถูกสร้างขึ้นโดยการจับคู่แคโทด PBA ที่มีน้ำต่ำกับสารเติมแต่ง Na2C2O4 และแอโนดคาร์บอนแข็ง (HC) ภายในไดอะคริเลตโพลี (เอทิลีนไกลคอล) (PEGDA) อิเล็กโทรไลต์กึ่งโซลิดสเตตแบบพื้นฐาน ) ที่มีค่าการนำไฟฟ้าไอออนิกสูงและมีความเสถียรทางเคมีไฟฟ้า แบตเตอรี่นี้แสดงความจุเฉพาะตั้งแต่ 58 ถึง 105 mAh·g-1 ที่ความหนาแน่นปัจจุบันตั้งแต่ 20 ถึง 500 mA·g-1 ซึ่งสามารถรักษาการหมุนเวียนที่เสถียรได้นานกว่า 200 รอบ การศึกษาครั้งนี้เน้นย้ำถึงการปรับปรุงที่สำคัญในด้านความเสถียรและความสามารถของวัสดุแคโทด PBA โดยการกำจัดน้ำที่เป็นผลึกในวัสดุเหล่านั้นอย่างมีประสิทธิภาพ
คำสำคัญ: แบตเตอรี่นาไอออน; แบตเตอรี่กึ่งโซลิดสเตต แคโทดสีน้ำเงินปรัสเซียน; การวิเคราะห์ในแหล่งกำเนิด
การพัฒนาเทคโนโลยีแบตเตอรี่ประสิทธิภาพสูงถือเป็นความต้องการเชิงกลยุทธ์ที่สำคัญสำหรับจีนในการเปลี่ยนแปลงและอัปเกรดโครงสร้างพลังงาน ส่งเสริมเศรษฐกิจสะอาดที่มีคาร์บอนต่ำ และบรรลุเป้าหมาย "ความเป็นกลางของคาร์บอนและจุดสูงสุดของคาร์บอน" แบตเตอรี่ลิเธียมไอออนเป็นหนึ่งในระบบแบตเตอรี่ประสิทธิภาพสูงที่ใช้กันอย่างแพร่หลายที่สุด อย่างไรก็ตาม ความอุดมสมบูรณ์ของลิเธียมในเปลือกโลกมีเพียง 0.0065% ทรัพยากรลิเธียมของจีนมีสัดส่วนเพียง 7% ของทั้งหมดของโลก และเกือบ 70% ของลิเธียมคาร์บอเนตนำเข้า ในอนาคตคงเป็นเรื่องยากที่จะตอบสนองความต้องการมหาศาลในด้านการจัดเก็บพลังงานและแบตเตอรี่สำรอง ปริมาณโซเดียมในเปลือกโลกสูงกว่าลิเธียมถึง 400 เท่า ปริมาณสำรองโซเดียมของจีนคิดเป็นประมาณ 22% ของปริมาณสำรองทั้งหมดของโลก จากมุมมองของต้นทุนวัตถุดิบ ต้นทุนของแบตเตอรี่โซเดียมไอออนสามารถลดลงได้ 30% ถึง 40% เมื่อเทียบกับแบตเตอรี่ลิเธียมไอออน นอกจากนี้ เมื่อเปรียบเทียบกับแบตเตอรี่ลิเธียมไอออนแล้ว แบตเตอรี่โซเดียมไอออนยังมีประสิทธิภาพที่อุณหภูมิต่ำได้ดีกว่า ช่วงอุณหภูมิการทำงานที่กว้างขึ้น และมีความปลอดภัยสูงกว่า ข้อได้เปรียบที่เป็นเอกลักษณ์เหล่านี้ทำให้พวกเขามุ่งความสนใจไปที่การใช้งานการจัดเก็บพลังงานที่คำนึงถึงต้นทุนและมีความสำคัญต่อความปลอดภัย [1]
ด้วยเป้าหมาย "คาร์บอนคู่" ความต้องการของจีนในด้านการจัดเก็บพลังงานและแบตเตอรี่พลังงานจึงสูงถึง 158.5 GWh ในปี 2563 และความต้องการแบตเตอรี่ของโลกคาดว่าจะเข้าสู่ยุค TWh ในปี 2568 ด้วยความก้าวหน้าของเทคโนโลยีแบตเตอรี่ ความหนาแน่นของพลังงานของ แบตเตอรี่ได้เพิ่มขึ้นอย่างรวดเร็ว และข้อกำหนดด้านความปลอดภัยของแบตเตอรี่ก็มีความโดดเด่นมากขึ้น แบตเตอรี่ลิเธียม/โซเดียมไอออนแบบดั้งเดิมใช้อิเล็กโทรไลต์อินทรีย์เหลวซึ่งมีแนวโน้มที่จะเกิดการรั่วไหล ซึ่งจะลดความน่าเชื่อถือของแบตเตอรี่ [2-3] การใช้แบตเตอรี่โซลิดสเตตที่มีความเสถียรทางเทอร์โมอิเล็กทริกสูง ความแข็งแรงเชิงกลสูง และไม่มีความเสี่ยงต่อการรั่วซึมเป็นแนวทางที่เป็นไปได้ในการแก้ปัญหาความน่าเชื่อถือ [4-5] แต่มีปัญหาเช่นความหนาแน่นสูงของอิเล็กโทรไลต์ของแข็ง ต่ำ การนำไอออนและการสัมผัสกับส่วนต่อประสาน "ของแข็ง-ของแข็ง" ของอิเล็กโทรดไม่ดี [6] อิเล็กโทรไลต์เสมือนของแข็งระหว่างของเหลวและของแข็งมีเสถียรภาพและความปลอดภัยดีกว่าอิเล็กโทรไลต์เหลว และเหนือกว่าอิเล็กโทรไลต์ที่เป็นของแข็งในแง่ของการนำไอออน ความยืดหยุ่น และความเข้ากันได้ของอินเทอร์เฟซ [7⇓-9] ข้อดีเหล่านี้ทำให้แบตเตอรี่กึ่งโซลิดสเตตเป็นหนึ่งในทิศทางการโฟกัสที่เป็นไปได้มากขึ้นในด้านเทคโนโลยีแบตเตอรี่ขั้นสูง
ปัจจุบันสารประกอบสีน้ำเงินปรัสเซียน (PBA) เป็นวัสดุแคโทดที่ได้รับความนิยมมากที่สุดสำหรับแบตเตอรี่โซเดียมไอออน โครงสร้างโครงกระดูกแบบเปิดและตำแหน่งกักเก็บโซเดียมที่อุดมสมบูรณ์ทำให้มีความจุจำเพาะทางทฤษฎีสูง (170 mAh g-1) และประสิทธิภาพการขนส่งไอออนที่ดี [10-11] ในแบตเตอรี่โซลิดสเตต PBA ไม่เพียงแต่สามารถใช้เป็นวัสดุแคโทดเท่านั้น แต่ยังสามารถใช้เป็นอิเล็กโทรไลต์ของแข็ง [12-13] ได้อีกด้วย อย่างไรก็ตาม โดยทั่วไป PBA จะถูกเตรียมโดยการตกตะกอนของสารละลาย ซึ่งจะทำให้เกิดข้อบกพร่องที่ว่างของ Fe(CN)64- และน้ำคริสตัลจำนวนมากในโครงสร้าง ขัดขวางการฝัง Na+ ลงในโครงข่าย PBA และจำกัดความสามารถในการกักเก็บโซเดียมของพวกมัน . นอกจากนี้ น้ำคริสตัลใน PBA จะค่อยๆ ปล่อยเข้าสู่อิเล็กโทรไลต์ในระหว่างปฏิกิริยาของแบตเตอรี่ ส่งผลให้ประสิทธิภาพของแบตเตอรี่ลดลงอย่างรวดเร็ว ปฏิกิริยาข้างเคียง อาการท้องอืด และปัญหาอื่นๆ [11,14] ปัญหาเหล่านี้จำกัดการใช้ PBA ในแบตเตอรี่โซลิดสเตต และทำให้ยากต่อการจับคู่กับอิเล็กโทรไลต์ของแข็งอนินทรีย์ที่ไวต่อน้ำส่วนใหญ่ การก่อตัวของข้อบกพร่องที่ว่างและน้ำที่เป็นผลึกใน PBA สามารถยับยั้งได้อย่างมีประสิทธิภาพโดยใช้กลยุทธ์ต่างๆ เช่น การบำบัดด้วยความร้อนใต้พิภพ[15] การตกตะกอนร่วมอย่างช้าๆ[16] การยับยั้ง Fe2+ ออกซิเดชัน[17] การกัดด้วยสารเคมี[18] และ การเติมองค์ประกอบ[19-20] อย่างไรก็ตาม กระบวนการทางเทคนิคที่เกี่ยวข้องนั้นซับซ้อนและยากต่อการควบคุมอย่างแม่นยำ และประสิทธิภาพของแคโทด PBA ที่ได้รับก็จำเป็นต้องได้รับการปรับปรุงเช่นกัน จากปัญหาข้างต้น การศึกษานี้เสนอวิธีการบำบัดความร้อนที่ง่ายและมีประสิทธิภาพเพื่อลดปริมาณน้ำที่เป็นผลึกใน PBA และปรับปรุงความเสถียรในการจัดเก็บโซเดียม ด้วยเทคโนโลยีโพลีเมอไรเซชันในแหล่งกำเนิด ทำให้อิเล็กโทรไลต์แข็งที่เป็นเกณฑ์มาตรฐานของโพลีเอทิลีนไกลคอลไดอะคริเลต (PEGDA) มีค่าการนำไฟฟ้าไอออนสูงและมีความเสถียรทางเคมีไฟฟ้าสูงได้รับการพัฒนา บนพื้นฐานนี้ แคโทด PBA ที่มีน้ำต่ำและแอโนดคาร์บอนแข็ง (HC) ถูกจับคู่ในอิเล็กโทรไลต์แข็งมาตรฐาน PEGDA และ Na2C2O4 ถูกเติมลงในแคโทดในฐานะตัวชดเชยโซเดียมแบบเสียสละตัวเองเพื่อสร้างเสมือนประสิทธิภาพสูง แบตเตอรี่โซเดียมไอออนโซลิดสเตต กลไกการจัดเก็บโซเดียมแบบไดนามิกของแคโทด PBA และแอโนด HC ถูกเปิดเผยโดยเทคโนโลยีการวิเคราะห์ในแหล่งกำเนิด
1 วิธีการทดลอง
1.1 การเตรียมแคโทด PBA ที่มีน้ำต่ำ
โซเดียมซิเตรต 116 มิลลิโมลและ FeSO4·7H2O 24 มิลลิโมลถูกละลายในน้ำปราศจากไอออนที่ปราศจากออกซิเจน 400 มิลลิลิตร โซเดียมซิเตรต 116 มิลลิโมลและ Na4Fe(CN)6 26 มิลลิโมลถูกละลายในน้ำปราศจากไอออนที่ถูกดีออกซิเจน 400 มิลลิลิตร สารละลายที่มี FeSO4 ถูกเติมอย่างช้าๆ ไปยังสารละลายที่มี Na4Fe(CN)6 และปฏิกิริยาถูกกวนที่อุณหภูมิคงที่เป็นเวลา 6 ชั่วโมง ล้างผลิตภัณฑ์สามครั้งโดยการปั่นแยกด้วยเอทานอลและน้ำปราศจากไอออนที่ถูกดีออกซิเจน และถูกทำให้แห้งในสุญญากาศที่ 120 องศาเป็นเวลา 24 ชั่วโมงเพื่อให้ได้ PBA ที่มีปริมาณน้ำที่เป็นผลึกสูง (Hw-PBA) มันถูกวางไว้ในเตาหลอมหลอดที่มีการป้องกันอาร์กอน และเผาที่ 270 องศาเป็นเวลา 2 ชั่วโมงเพื่อให้ได้ PBA ที่มีน้ำต่ำ (Lw-PBA) โดยมีอัตราการให้ความร้อน 0.5 องศา ·นาที-1
1.2 การแสดงลักษณะตัวอย่าง
วิเคราะห์สัณฐานวิทยาและโครงสร้างของตัวอย่างโดยใช้กล้องจุลทรรศน์อิเล็กตรอนแบบสแกนการแผ่รังสีภาคสนาม องค์ประกอบทางเคมีของตัวอย่างได้รับการวิเคราะห์โดยใช้เครื่องเอ็กซ์เรย์โฟโตอิเล็กตรอนสเปกโตรมิเตอร์และสเปกโตรมิเตอร์การปล่อยพลาสมาแบบเหนี่ยวนำคู่ แบตเตอรี่ได้รับการวิเคราะห์ในแหล่งกำเนิดโดยใช้เครื่องเอ็กซ์เรย์ดิฟแฟรกโตมิเตอร์แบบผงและเลเซอร์รามันสเปกโทรสโกปี ปริมาณน้ำคริสตัลตัวอย่างได้รับการวิเคราะห์โดยใช้เครื่องวิเคราะห์เทอร์โมกราวิเมตริกในบรรยากาศอาร์กอนที่อัตราการให้ความร้อน 10 องศา ·นาที-1
1.3 การประกอบแบตเตอรี่และการทดสอบประสิทธิภาพเคมีไฟฟ้า
1.3.1 ส่วนประกอบโซเดียมเหลวแบบครึ่งแบตเตอรี่
CR20มีการประกอบเซลล์ปุ่ม 16 เซลล์สำหรับการทดสอบ วัสดุแคโทดสีน้ำเงินปรัสเซียน (Hw-PBA หรือ Lw-PBA), Ketjen black (KB) และสารยึดเกาะโพลีไวนิลิดีนฟลูออไรด์ (PVDF) ถูกผสมอย่างสม่ำเสมอในอัตราส่วนมวล 8:1:1, N-เมทิลไพโรลิโดน (NMP) ถูกเติมเป็น ตัวทำละลายและสารช่วยกระจายตัว และสารละลายที่ได้จะถูกเคลือบอย่างสม่ำเสมอบนฟอยล์อลูมิเนียมเคลือบคาร์บอนเป็นแคโทด โดยมีการโหลดวัสดุที่ใช้งานอยู่ 3~4 มก.·ซม.{{10}} แผ่นโลหะโซเดียมถูกใช้เป็นอิเล็กโทรดเคาน์เตอร์และอิเล็กโทรดอ้างอิง อิเล็กโทรไลต์คือสารละลาย DMC/EC (DMC: ไดเมทิลคาร์บอเนต, EC: เอทิลีนคาร์บอเนต, อัตราส่วนปริมาตร 1:1) ของ NaClO4 1.0 โมล·L-1 และฟลูออโรเอทิลีนคาร์บอเนต (FEC) 5.0% แบตเตอรี่ถูกประกอบในกล่องถุงมือที่เติมอาร์กอน (ปริมาณน้ำ<10-7, oxygen content <10-7).
1.3.2 ชุดประกอบแบตเตอรี่โซเดียมเหลวแบบเต็ม
อิเล็กโทรดบวกถูกเตรียมโดยใช้วิธีการข้างต้น HC ถูกใช้เป็นอิเล็กโทรดเชิงลบ และอัตราส่วน N/P ของอิเล็กโทรดบวกและลบถูกควบคุมที่ 1.1~1.2 แบตเตอรี่ถูกประกอบในกล่องถุงมือที่เต็มไปด้วยอาร์กอน (ปริมาณน้ำ<10-7, oxygen content <10-7) using the above electrolyte.
1.3.3 การเตรียมอิเล็กโทรไลต์เสมือนของแข็ง
PEGDA ถูกผสมกับอิเล็กโทรไลต์ของเหลวข้างต้นที่อัตราส่วนมวล 7:93 5.0% อะโซบิไอโซบิวไทโรไนไตรล์ (AIBN) ถูกเติมเป็นตัวเริ่มปฏิกิริยาโพลีเมอไรเซชันเพื่อสร้างสารละลายตั้งต้นของอิเล็กโทรไลต์เสมือนของแข็ง สารละลายนี้ถูกให้ความร้อนที่ 60 องศา เป็นเวลา 10 ชั่วโมงเพื่อก่อรูปอิเล็กโทรไลต์เสมือนของแข็ง
1.3.4 การประกอบแบตเตอรี่โซเดียมไอออนกึ่งโซลิดสเตตเต็ม
วัสดุอิเล็กโทรดเชิงบวก สารเสริมโซเดียม Na2C2O4 สารนำไฟฟ้า KB และสารยึดเกาะ PVDF ได้รับการผสมอย่างสม่ำเสมอในอัตราส่วนมวล 6.4: 1.6: 1.0: 1.0 มีการเติม NMP เป็นตัวทำละลายและ สารช่วยกระจายตัวและสารละลายที่ได้รับถูกเคลือบอย่างสม่ำเสมอบนฟอยล์อลูมิเนียมเคลือบคาร์บอนเป็นอิเล็กโทรดบวก โดยมีการโหลดวัสดุที่ใช้งานอยู่ที่ 3 ~ 4 มก.·ซม.-2 HC ถูกใช้เป็นอิเล็กโทรดเชิงลบ และอัตราส่วน N/P ของอิเล็กโทรดบวกและลบถูกควบคุมที่ 1.1~1.2 เติมสารละลายตั้งต้นของอิเล็กโทรไลต์เสมือนของแข็งลงในแบตเตอรี่ และหลังจากที่แบตเตอรี่ถูกห่อหุ้มแล้ว ก็จะถูกให้ความร้อนที่ 60 องศาเป็นเวลา 10 ชั่วโมงเพื่อให้ได้แบตเตอรี่เสมือนโซลิดสเตต แบตเตอรี่ถูกประกอบในกล่องถุงมือที่เต็มไปด้วยอาร์กอน (ปริมาณน้ำ<10-7, oxygen content <10-7).
1.3.5 การทดสอบประสิทธิภาพของแบตเตอรี่
ค่าการนำไฟฟ้าไอออนิกของอิเล็กโทรไลต์เสมือนของแข็งได้รับการทดสอบโดยสเปกโทรสโกปีอิมพีแดนซ์เคมีไฟฟ้า (EIS) โดยใช้เวิร์กสเตชันเคมีไฟฟ้า ช่วงความถี่ทดสอบคือ 1 Hz~1000 kHz และแอมพลิจูดของแรงดันรบกวนคือ 5.0 mV หน้าต่างความเสถียรทางเคมีไฟฟ้าของอิเล็กโทรไลต์เสมือนของแข็งได้รับการทดสอบโดยโวลแทมเมทรีเชิงเส้น (LSV) ด้วยอัตราการกวาดที่ 5 มิลลิโวลต์·วินาที-1 ศึกษาประสิทธิภาพของวัสดุและแบตเตอรี่โดยวิธีประจุและคายประจุกระแสคงที่โดยใช้เครื่องทดสอบแบตเตอรี่ Land CT2001A หน้าต่างแรงดันไฟฟ้าแบบครึ่งเซลล์คือ 2.0~3.8 V (เทียบกับ Na/Na+) หน้าต่างแรงดันไฟฟ้าแบบเต็มเซลล์คือ 1.5~ 3.8 V และความหนาแน่นกระแสคือ 10~500 mA·g-1 เมื่อทดสอบความเสถียรของวงจร ขั้นแรกให้หมุนแบตเตอรี่ 5 ครั้งที่ความหนาแน่นกระแส 50 mA·g-1 จากนั้นทำการทดสอบความเสถียรของวงจรที่ความหนาแน่นกระแสต่างกัน
2 ผลลัพธ์และการสนทนา
2.1 สัณฐานวิทยาและการวิเคราะห์องค์ประกอบ
เส้นโค้ง TGA ของ Hw-PBA ในรูปที่ 1(a) แสดงสองบริเวณที่มีการลดน้ำหนักอย่างรวดเร็ว: 1) อุณหภูมิห้องอยู่ที่ 270 องศา 2) 440 ถึง 580 องศา ในพื้นที่เดิม น้ำหนักที่ลดลงจากอุณหภูมิห้องเป็น 120 องศา (เศษส่วนมวล 3.1%) เกิดจากการเอาน้ำที่ถูกดูดซับออก การสูญเสียน้ำหนักจาก 120 ถึง 200 องศา (เศษส่วนมวล 6.10%) เกิดจากการกำจัดน้ำคั่นในโครงสร้างกรอบ PBA การลดน้ำหนักจาก 200 ถึง 270 องศา (เศษส่วนมวล 6.89%) สอดคล้องกับการกำจัดน้ำคริสตัลใน PBA ดังนั้นจึงเลือกใช้ความร้อน 270 องศาเพื่อขจัดน้ำออกจาก Hw-PBA หลังจากการอบชุบด้วยความร้อนที่อุณหภูมินี้ Lw-PBA ที่ได้รับจะสูญเสียน้ำหนักเพียงประมาณ 1.18% ที่อุณหภูมิห้อง ~270 องศา ซึ่งต่ำกว่า Hw-PBA ถึง 92.67% และลดน้ำหนักได้ประมาณ 0.74% ที่ 200~270 องศา ซึ่งต่ำกว่า Hw-PBA ถึง 89.26% ผลลัพธ์ข้างต้นแสดงให้เห็นว่าการบำบัดความร้อนสามารถกำจัดน้ำประเภทต่างๆ ใน PBA ได้อย่างมีประสิทธิภาพ และ PBA ที่มีปริมาณน้ำต่ำที่ได้รับจะมีเสถียรภาพทางความร้อนที่ดี

รูปที่ 1 การวิเคราะห์ TGA สัณฐานวิทยา และโครงสร้างของแคโทด PBA
(a) เส้นโค้ง TGA และ (b) รูปแบบ XRD ของ Hw-PBAs และ Lw-PBAs; (cf) รูปภาพ SEM ของ (c, d) Hw-PBA และ (e, f) Lw-PBA
รูปที่ 1(b) แสดงสเปกตรัม XRD ของ Hw-PBA และ Lw-PBA ยอดการเลี้ยวเบนของ Hw-PBA ที่ 2θ=17.0 องศา , 24.0 องศา และ 34.4 องศา สอดคล้องกับผลึก (012), (220) และ (024) เครื่องบินตามลำดับ หลังจากการอบชุบด้วยความร้อน ยอดการเลี้ยวเบนที่สอดคล้องกับระนาบคริสตัล (024) จะหายไป ซึ่งบ่งชี้ว่าน้ำคริสตัลถูกกำจัดออกได้สำเร็จ และตำแหน่งยอดการเลี้ยวเบนที่สอดคล้องกับระนาบคริสตัล (012) และ (220) เคลื่อนที่ไปยังมุมที่สูงขึ้น ซึ่งบ่งชี้ว่า ปริมาตรเซลล์หน่วยจะลดลงหลังจากที่น้ำคริสตัลถูกกำจัดออกไป นอกจากนี้ ยอดการเลี้ยวเบนใหม่จะปรากฏที่ 2θ=27.1 องศา , 30.7 องศา และ 36.9 องศา ซึ่งบ่งชี้ว่ามีโครงสร้างผลึกสามเหลี่ยมเกิดขึ้นหลังจากการอบชุบด้วยความร้อน การวิเคราะห์ SEM (รูปที่ 1(c~e)) แสดงให้เห็นว่า Hw-PBA และ Lw-PBA มีสัณฐานวิทยาลูกบาศก์ที่คล้ายกันโดยมีขนาดเฉลี่ย 2~3 µm พื้นผิวของอนุภาค Lw-PBA ที่ได้รับหลังการบำบัดความร้อนมีความหยาบเล็กน้อย (รูปที่ 1(f)) แต่เนื่องจากอุณหภูมิการบำบัดด้วยความร้อนต่ำ จึงไม่มีการหลอมละลายและการจับตัวเป็นก้อนอย่างเห็นได้ชัดเกิดขึ้น องค์ประกอบของ Lw-PBA ได้รับการประมาณค่าไว้ที่ Na1.91Fe- [Fe(CN)6]·3.2H2O โดยการวิเคราะห์ปริมาณธาตุโลหะโดย ICP-OES และวัดปริมาณน้ำโดย TGA
เพื่อสำรวจองค์ประกอบและโครงสร้างทางเคมีของ Hw-PBA และ Lw-PBA เพิ่มเติม ได้ทำการวิเคราะห์ XPS ในสเปกตรัม Fe2p XPS ความละเอียดสูงของ Hw-PBA พีคลักษณะเฉพาะสองตัวที่พลังงานการจับที่ 708.6 และ 721.4 eV สอดคล้องกับ Fe(II) และ Fe(III) ตามลำดับ (รูปที่ 2(a) ). Fe(II) และ Fe(III) มีอยู่ใน Lw-PBA เช่นกัน แต่สัดส่วนของ Fe(III) เพิ่มขึ้นอย่างมีนัยสำคัญ (รูปที่ 2(b)) นี่เป็นเพราะว่า [NaH2O]+ ถูกเอาออกจากโครงสร้าง PBA ในระหว่างกระบวนการบำบัดความร้อน และ Fe(II) ใน Lw-PBA ถูกออกซิไดซ์บางส่วนเพื่อรักษาสมดุลของเวเลนซ์ ในสเปกตรัม O1s XPS ความละเอียดสูงของ Hw-PBA จุดสูงสุดของลักษณะเฉพาะที่พลังงานยึดเหนี่ยว 536.0, 533.7, 531.9 และ 529.7 eV สอดคล้องกับน้ำคั่นระหว่างหน้า น้ำที่ประสานกัน หมู่ไฮดรอกซิลที่พื้นผิว และสายพันธุ์ออกซิเจนใน โครงตาข่าย PBA ตามลำดับ (รูปที่ 2(c)) หลังจากการอบชุบด้วยความร้อน ยอดคุณลักษณะที่สอดคล้องกับน้ำที่ประสานกันจะหายไป ซึ่งบ่งชี้ว่ากระบวนการนี้สามารถกำจัดน้ำที่ประสานกันออกจาก Lw-PBA ได้อย่างมีประสิทธิภาพ (รูปที่ 2(d)) ในระหว่างกระบวนการนี้ Fe บนพื้นผิวของ PBA จะทำปฏิกิริยากับหมู่ไฮดรอกซิลเพื่อสร้างเหล็กออกไซด์ ส่งผลให้คุณลักษณะ Fe-O มีค่าสูงสุดที่พลังงานยึดเหนี่ยว 530.0 eV เพิ่มขึ้นอย่างมาก

รูปที่ 2 องค์ประกอบทางเคมีของแคโทด PBA
(a, b) สเปกตรัม Fe2p XPS ของ (a) Hw-PBAs และ (b) Lw-PBAs; (c, d) สเปกตรัม XPS ของ O1s ของ (c) Hw-PBA และ (d) Lw-PBA
2.2 สมรรถนะทางเคมีไฟฟ้า
รูปที่ 3(a) แสดงเส้นโค้งวงจรประจุ-คายประจุกระแสคงที่ของครึ่งเซลล์โซเดียมไอออนที่มี Hw-PBA และ Lw-PBA เป็นอิเล็กโทรดบวกที่ความหนาแน่นกระแส 100 mA·g -1 โดยมีหน้าต่างแรงดันไฟฟ้า 2.0~3.8 V (เทียบกับ Na/Na+) หลังจากรอบการคายประจุ 340 รอบ อิเล็กโทรดขั้วบวก Lw-PBAs ยังสามารถรักษาความจุจำเพาะสูงไว้ที่ 91 mAh·g-1 โดยมีอัตราการคงความจุอยู่ที่ 88% และอัตราการสูญเสียความสามารถในการคายประจุครั้งเดียวโดยเฉลี่ย เพียง 0.035% แสดงความเสถียรของวงจรที่ดีเยี่ยม ภายใต้เงื่อนไขการปล่อยประจุเดียวกัน อัตราการรักษาความจุของอิเล็กโทรดขั้วบวก Hw-PBAs โดยไม่ต้องกำจัดน้ำคริสตัลจะอยู่ที่เพียง 73% ซึ่งแสดงให้เห็นถึงบทบาทที่สำคัญในการขจัดน้ำคริสตัลในการปรับปรุงความเสถียรของวงจรของอิเล็กโทรดขั้วบวกของ PBA รูปที่ 3(b) แสดงเส้นโค้งประจุ-คายประจุกระแสคงที่ของแคโทด Lw-PBAs ที่ความหนาแน่นกระแส 100 mA·g-1 แสดงคุณลักษณะแพลตฟอร์มแรงดันไฟฟ้าคู่ทั่วไป: (1) แพลตฟอร์มแรงดันไฟฟ้าประมาณ 3.2 V สอดคล้องกับกระบวนการรีดอกซ์ของ Fe2+/Fe3+ หมุนต่ำ (พิกัดกับ C); (2) แพลตฟอร์มแรงดันไฟฟ้าประมาณ 2.9 V สอดคล้องกับกระบวนการรีดอกซ์ของ Fe2+/Fe3+ สปินสูง (พิกัดกับ N) การปรากฏตัวของแท่นแรงดันไฟฟ้าที่ประมาณ 3.2 V บ่งชี้ว่าการกำจัดน้ำคริสตัลออกมีประโยชน์ในการเสริมปฏิกิริยารีดอกซ์ของ Fe2+/Fe3+ สปินต่ำใน PBA ซึ่งช่วยปรับปรุงโซเดียมของ PBA ความจุ ในกระบวนการวงจรต่อมา กราฟประจุ-คายประจุของแคโทด Lw-PBA ยังคงสม่ำเสมอ โดยแสดงความเสถียรทางโครงสร้างที่ดี ที่ความหนาแน่นปัจจุบันที่ 10, 50, 100, 200 และ 500 mA·g-1 แคโทด Lw-PBAs สามารถรักษาความจุเฉพาะที่สามารถพลิกกลับได้สูงที่ 126, 112, 110, 108 และ 107 mAh·g{{ 60}} (รูปที่ 3(c)) โดยเฉพาะอย่างยิ่ง ที่ความหนาแน่นกระแสสูงที่ 500 mA·g-1 แคโทด Lw-PBA มีการกักเก็บความจุที่ดีเยี่ยม และความจุจำเพาะของแคโทดนั้นสูงกว่า Hw-PBA ประมาณ 13.4% เมื่อความหนาแน่นกระแสลดลงกลับไปเป็น 10 mA·g-1 ความจุจำเพาะของแคโทด Lw-PBAs จะสามารถคืนสภาพเป็น 125 mAh·g-1 ซึ่งใกล้เคียงกับความจุจำเพาะเริ่มต้น ซึ่งบ่งชี้ว่า สามารถรักษาเสถียรภาพของโครงสร้างที่ดีเยี่ยมในระหว่างการเก็บรักษาโซเดียมอย่างรวดเร็ว

รูปที่ 3 สมรรถนะทางเคมีไฟฟ้าของแคโทด PBA ในครึ่งเซลล์ Na-ion
(a) ประสิทธิภาพการปั่นจักรยานของแคโทด Lw-PBAs และ Hw-PBAs ที่ความหนาแน่นกระแส 100 mA ·g -1; (b) เส้นโค้งประจุ-คายประจุของแคโทด Lw-PBAs ที่ 100 mA·g-1; (c) ความสามารถด้านอัตราของแคโทด Lw-PBA และ Hw-PBAs ที่ความหนาแน่นกระแสต่างๆ ตั้งแต่ 10 mA·g-1 ถึง 500 mA·g-1; หน้าต่างแรงดันไฟฟ้าคือ 2.0-3.8 V (เทียบกับ Na/Na+) สำหรับการทดสอบแบบครึ่งเซลล์ทั้งหมด มีรูปสีสันสดใสอยู่บนเว็บไซต์
2.3 การวิเคราะห์กลไกการเก็บโซเดียมในแหล่งกำเนิด
อิเล็กโทรดบวก Lw-PBAs จับคู่กับอิเล็กโทรดลบ HC และสารละลาย DMC/EC ที่มี 1.0 โมล·L-1 NaClO4 และ 5.0% FEC โดยมวลคือ ใช้เป็นอิเล็กโทรไลต์เหลว (LE) เพื่อประกอบแบตเตอรี่เต็ม (Lw-PBAs|LE|HC, รูปที่ 4(a)) ศึกษาการเปลี่ยนแปลงโครงสร้างแบบไดนามิกของวัสดุอิเล็กโทรดบวกและลบของแบตเตอรี่เต็มในระหว่างปฏิกิริยาประจุและคายประจุโดยใช้เทคโนโลยีการวิเคราะห์ในแหล่งกำเนิด การวิเคราะห์ XRD ในแหล่งกำเนิดของอิเล็กโทรดบวก Lw-PBA แสดงให้เห็นว่าหลังจากที่แรงดันไฟฟ้าในการชาร์จเพิ่มขึ้นเป็น 3.2 V ยอดการเลี้ยวเบนที่สอดคล้องกับ (110) และ (104) จะค่อยๆ รวมเข้าด้วยกันเพื่อสร้างจุดสูงสุดแบบกว้าง (รูปที่ 4(b) ). ปรากฏการณ์นี้สอดคล้องกับกระบวนการที่ Na+ หลุดออกจากอิเล็กโทรดบวกของ Lw-PBAs ทำให้โครงสร้างผลึกเปลี่ยนจากโครงสร้างสามเหลี่ยมไปเป็นโครงสร้างลูกบาศก์[21] ในระหว่างกระบวนการคายประจุ ไม่พบการแบ่งพีคกว้างๆ ออกเป็นพีคการเลี้ยวเบน (110) และ (104) ใหม่ ซึ่งบ่งชี้ว่ากระบวนการเปลี่ยนเฟสไม่สามารถย้อนกลับได้ ส่งผลให้เกิดการสูญเสียประสิทธิภาพคูลอมบิกครั้งแรก นอกจากนี้ ในระหว่างกระบวนการชาร์จและคายประจุครั้งแรกของอิเล็กโทรดลบ HC ฟิล์มระหว่างเฟสของอิเล็กโทรไลต์แข็ง (SEI) ที่เกิดขึ้นบนพื้นผิวทำให้เกิดการสูญเสียลิเธียมที่ไม่สามารถย้อนกลับได้ (18%) ซึ่งเป็นหนึ่งในเหตุผลของประสิทธิภาพคูลอมบิกครั้งแรกด้วย การสูญเสียแบตเตอรี่ทั้งหมด (รูปที่ 4 (c, d))
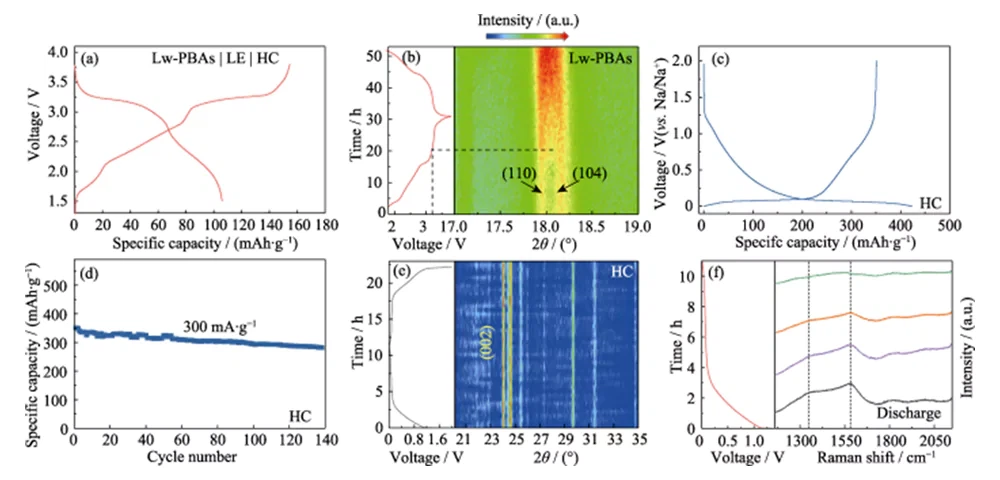
รูปที่ 4 การวิเคราะห์ในแหล่งกำเนิดของกลไกการจัดเก็บ Na สำหรับแคโทด Lw-PBA และแอโนด HC
( a ) เส้นโค้งการชาร์จและคายประจุของ Lw-PBAs|LE|HC เต็มเซลล์; ( b ) รูปแบบ XRD ในแหล่งกำเนิด ของแคโทด Lw-PBAs ระหว่างการทำงานของเซลล์เต็ม; (c) เส้นโค้งประจุ-คายประจุสำหรับรอบแรกและ (d) ความเสถียรในการหมุนเวียนของขั้วบวก HC ที่ความหนาแน่นกระแส 300 mA·g-1; ( e ) รูปแบบ XRD ในแหล่งกำเนิด และ ( f ) สเปกตรัม Raman ในแหล่งกำเนิดของแอโนด HC ระหว่างการทำงานของเซลล์เต็ม มีรูปสีสันสดใสอยู่บนเว็บไซต์
ในสเปกตรัม XRD ในแหล่งกำเนิดของแอโนด HC ไม่มีการสังเกตการเปลี่ยนแปลงพีคที่ชัดเจน (002) ในระหว่างกระบวนการประจุและคายประจุ ซึ่งบ่งชี้ว่า Na+ ไม่ได้ถูกแทรกเข้าไปในชั้นโครงสร้างกราไฟต์ และไม่มีการสังเกตพีคของการเลี้ยวเบนจากโลหะโซเดียม ( รูปที่ 4(จ)) ดังนั้น ความสามารถในการกักเก็บโซเดียมของแอโนด HC อาจเกิดจากการดูดซับและการเติม Na+ ในบริเวณที่มีข้อบกพร่องและรูขุมขนของ HC มาก แทนที่จะเป็นการแทรกซึมของ Na+ หรือการตกตะกอนของโซเดียมโลหะ [22] เพื่อศึกษากลไกปฏิกิริยาการเก็บโซเดียมใน HC เพิ่มเติม การวิเคราะห์รามานในแหล่งกำเนิดได้ดำเนินการบนขั้วลบของ HC ในระหว่างกระบวนการประจุและคายประจุ (รูปที่ 4 (f)) อิเล็กโทรดลบ HC มียอดลักษณะรามานที่ชัดเจนที่ 1350 และ 1594 ซม.-1 พีคลักษณะเฉพาะที่มีเลขคลื่น 1350 ซม.-1 สอดคล้องกับการยืดการสั่นสะเทือนของโครงสร้างอะโรมาติกคาร์บอน (โหมด G) และพีคลักษณะเฉพาะที่มีเลขคลื่น 1594 ซม.-1 สอดคล้องกับคาร์บอนที่มีข้อบกพร่องที่ไม่เป็นระเบียบ โครงสร้าง (โหมด D) อัตราส่วนความเข้มของโหมด D และโหมด G (ID/IG) สามารถใช้เพื่อวัดระดับข้อบกพร่องและความผิดปกติของวัสดุคาร์บอน ในระหว่างกระบวนการคายประจุ ID/IG ของแอโนด HC จะลดลงตามการแทรกแซงของ Na+ อย่างต่อเนื่อง ซึ่งบ่งชี้ว่าพฤติกรรมการดูดซับที่มีนัยสำคัญของ Na+ ที่ตำแหน่งที่มีข้อบกพร่องนั้นเป็นแหล่งที่มาหลักของความจุโซเดียมของแอโนด HC
2.4 โครงสร้างและประสิทธิภาพของเซลล์เต็มเซลล์กึ่งโซลิดสเตต
ประสิทธิภาพคูลอมบิกครั้งแรกของโซเดียมไอออนเต็มเซลล์ที่สร้างโดยใช้อิเล็กโทรดบวก Lw-PBA และอิเล็กโทรดลบ HC อยู่ที่ 67.3% เท่านั้น (รูปที่ 4(a)) เพื่อแก้ไขปัญหานี้ Na2C2O4 ที่เป็นมิตรต่อสิ่งแวดล้อม เป็นพิษต่ำ และมีความเสถียรในอากาศ ถูกใช้เป็นตัวชดเชยโซเดียมแบบเสียสละตัวเองในอิเล็กโทรดบวก Lw-PBAs เพื่อปรับปรุงประสิทธิภาพคูลอมบิกแรกของเซลล์เต็ม [23] ขนาดอนุภาคของ Na2C2O4 เชิงพาณิชย์มากกว่าหลายร้อยไมครอนและมีฤทธิ์ทางเคมีไฟฟ้าต่ำ ดังนั้นจึงนำไปตกผลึกใหม่เพื่อให้ได้ Na2C2O4 ที่มีขนาดอนุภาคหลายไมครอน (รูปที่ 5(a)) Na2C2O4 ขนาดไมครอนสามารถปล่อยความจุจำเพาะสูงที่ 407 mAh·g−1 ในระหว่างกระบวนการชาร์จครั้งแรกภายในกรอบแรงดันไฟฟ้า 2.0~4.2 V ซึ่งชดเชยการสูญเสียความจุที่ไม่สามารถกลับคืนสภาพเดิมครั้งแรกของอิเล็กโทรดบวกได้อย่างมีประสิทธิภาพ (รูปที่ 5(ข)) ความจุจำเพาะการคายประจุเริ่มต้นของ Lw-PBAs|LE|HC เต็มเซลล์ด้วยการเติม Na2C2O4 (เศษส่วนมวล 20%) สามารถเข้าถึง 158 mAh·g-1 ซึ่งสูงกว่าความจุเต็มเซลล์ 92.7% โดยไม่มีการเติม Na2C2O4 (รูปที่ 5(c)) Lw-PBAs|LE|HC แบบเต็มเซลล์ที่มีการเติม Na2C2O4 สามารถรักษาความจุจำเพาะแบบผันกลับได้ที่ 110, 101, 92, 87 และ 80 mAh·g-1 ที่ความหนาแน่นปัจจุบันที่ 10, 50, 100, 200 และ 500 mA·g-1 (รูปที่ 5(d)) ที่ความหนาแน่นกระแสสูงที่ 500 mA·g{-1 หลังจาก 1400 รอบที่เสถียร Lw-PBAs|LE|HC แบบเต็มเซลล์ที่มีการเติม Na2C2O4 สามารถรักษาความจุจำเพาะไว้ที่ 64 mAh·g{{71} } ซึ่งสูงกว่าเซลล์เต็มถึง 25.4% โดยไม่มีการเติม Na2C2O4 (รูปที่ 5(e))

รูปที่ 5 ผลของ Na2C2O4 ต่อประสิทธิภาพเคมีไฟฟ้าของแคโทด Lw-PBAs
(a) ภาพ SEM และ (b) เส้นโค้งการคายประจุของ Na2C2O4 ด้วยขนาดไมโครมิเตอร์ที่ความหนาแน่นกระแส 180 mA·g-1; (c) เส้นโค้งประจุ-คายประจุของ Lw-PBAs|LE|HC เต็มเซลล์ที่มีหรือไม่มีการใช้ Na2C2O4 ที่ความหนาแน่นกระแส 100 mA·g-1; (d) ให้คะแนนประสิทธิภาพของ Lw-PBAs|LE|HC เต็มเซลล์ด้วย Na2C2O4 ที่ความหนาแน่นกระแสต่างๆ ตั้งแต่ 10 ถึง 500 mA·g-1; (e) ความเสถียรแบบวงรอบของ Lw-PBAs|LE|HC เต็มเซลล์โดยมีหรือไม่มีการใช้ Na2C2O4 ที่ความหนาแน่นกระแสขนาดใหญ่ที่ 500 mA·g-1; หน้าต่างแรงดันไฟฟ้าคือ 1.5-3.8 V สำหรับการทดสอบเต็มเซลล์ทั้งหมด มีรูปสีสันสดใสอยู่บนเว็บไซต์
บนพื้นฐานนี้ PEGDA ถูกผสมกับอิเล็กโทรไลต์ NaClO4 1.0 โมล·L-1 และอิเล็กโทรไลต์ DMC/EC โดยมีเศษส่วนมวล 5.0% FEC และ AIBN ถูกใช้เป็น ตัวริเริ่มปฏิกิริยาโพลีเมอไรเซชันด้วยความร้อนเพื่อพัฒนาอิเล็กโทรไลต์เสมือนของแข็ง (GPE) ประสิทธิภาพสูง เมื่อเปรียบเทียบกับ LE แล้ว GPE มีข้อดีตรงที่มีความเสี่ยงต่อการรั่วไหลน้อยกว่าและมีความผันผวนต่ำ สามารถคงความเสถียรที่แรงดันไฟฟ้าสูง 4.9 V (เทียบกับ Na/Na+) และมีช่วงเสถียรภาพทางเคมีไฟฟ้าที่กว้าง (รูปที่ 6(a)) เมื่อเปรียบเทียบกับอิเล็กโทรไลต์ที่เป็นของแข็ง GPE มีค่าการนำไฟฟ้าของไอออนิกและความเข้ากันได้ของอินเทอร์เฟซสูงกว่า และค่าการนำไฟฟ้าของไอออนิกที่อุณหภูมิห้องอยู่ที่ 3.51 mS·cm-1 (รูปที่ 6(b)) มันถูกจับคู่เพิ่มเติมกับอิเล็กโทรดบวก Lw-PBAs ที่มีปริมาณน้ำต่ำและอิเล็กโทรดลบ HC เพื่อสร้างแบตเตอรี่โซเดียมไอออนกึ่งของแข็งกึ่งของแข็ง (Lw-PBAs|GPE|HC) ที่ความหนาแน่นกระแส 100 mA·g{-1 ความจุจำเพาะการคายประจุครั้งแรกของแบตเตอรี่ Lw-PBAs|GPE|HC เสมือนโซลิดสเตตถึง 147.8 mAh·g-1 (รูปที่ 6(c )). ที่ความหนาแน่นปัจจุบัน 20, 50, 100, 200 และ 500 mA·g-1 สามารถรักษาความจุเฉพาะไว้ที่ 105, 94, 82, 70 และ 58 mAh·g-1 (รูปที่ 6( ง)) ที่ความหนาแน่นกระแส 100 mA·g-1 สามารถหมุนเวียนได้อย่างเสถียรมากกว่า 200 ครั้ง และประสิทธิภาพคูลอมบิกอยู่ใกล้กับ 100% (รูปที่ 6(e))

รูปที่ 6 สมรรถนะทางเคมีไฟฟ้าของฟูลเซลล์กึ่งโซลิดสเตตที่ใช้แคโทด Lw-PBA และ GPE ที่ใช้ PEGDA
(a) เส้นโค้ง LSV ที่อัตราการสแกน 5 mV·s-1; (ข) สเปกตรัม EIS; (c) เส้นโค้งประจุ-คายประจุที่ความหนาแน่นกระแส 100 mA·g-1; (d) ให้คะแนนประสิทธิภาพที่ความหนาแน่นปัจจุบันที่ 20-500 mA·g-1; (e) ประสิทธิภาพการปั่นจักรยานที่ 100 mA·g-1; หน้าต่างแรงดันไฟฟ้าคือ 1.5-3.8 V สำหรับการทดสอบเต็มเซลล์ทั้งหมด
3 บทสรุป
ในการศึกษานี้ วัสดุแคโทด PBA ที่มีปริมาณน้ำต่ำถูกเตรียมโดยวิธีการบำบัดความร้อนที่ง่ายและมีประสิทธิภาพ พบว่าการกำจัดน้ำคริสตัลไม่เพียงเพิ่มอัตราการกักเก็บความจุของแคโทด PBA จาก 73% เป็น 88% หลังจาก 340 รอบ แต่ยังช่วยเพิ่มความแข็งแกร่งให้กับปฏิกิริยารีดอกซ์ของ Fe2+/Fe ที่หมุนต่ำ 3+ ใน PBA ดังนั้นจึงปรับปรุงความสามารถในการกักเก็บโซเดียมของมัน กลไกการจัดเก็บโซเดียมแบบไดนามิกของแคโทด PBA และแอโนด HC ถูกเปิดเผยโดยเทคนิค Raman ในแหล่งกำเนิด และ XRD ในแหล่งกำเนิด การวิเคราะห์แสดงให้เห็นว่ากระบวนการของ Na+ ที่หลุดออกจากแคโทด PBA ทำให้โครงสร้างผลึกของมันเปลี่ยนจากลูกบาศก์สามมิติอย่างถาวร ส่งผลให้สูญเสียประสิทธิภาพคูลอมบิกแรก และการดูดซับของ Na+ ที่ตำแหน่งที่มีข้อบกพร่องเป็นแหล่งที่มาหลักของ ความจุโซเดียมของขั้วบวก HC หลังจากเติมตัวชดเชยโซเดียม Na2C2O4 (เศษส่วนมวล 20%) ลงในแคโทด ความสามารถในการคายประจุครั้งแรกของแคโทด PBA เพิ่มขึ้น 92.7% จากปฏิกิริยาโพลีเมอไรเซชันเชิงความร้อนของ PEGDA ที่ริเริ่มโดย AIBN อิเล็กโทรไลต์เสมือนของแข็งประสิทธิภาพสูงที่มีค่าการนำไฟฟ้าไอออนิกที่อุณหภูมิห้อง 3.51 mS·cm-1 และหน้าต่างความเสถียรทางเคมีไฟฟ้าขยายกว้างขึ้นเป็น 4.9 V (เทียบกับ Na/Na+) ที่พัฒนา. บนพื้นฐานนี้ แคโทด PBA ที่มีน้ำต่ำพร้อมตัวชดเชยโซเดียม Na2C2O4 ที่เพิ่ม, แอโนด HC และอิเล็กโทรไลต์โซลิดมาตรฐาน PEGDA ถูกรวมเข้าด้วยกันเพื่อสร้างแบตเตอรี่โซเดียมไอออนเสมือนโซลิดสเตตที่สามารถหมุนเวียนได้อย่างเสถียรมากกว่า 200 ครั้งที่ ความหนาแน่นกระแส 100 mA·g-1 การศึกษาพบว่าการกำจัดน้ำคริสตัลอย่างมีประสิทธิภาพเป็นวิธีที่จำเป็นในการปรับปรุงความเสถียรของวงจรของแคโทด PBA และตระหนักถึงการสร้างแบตเตอรี่โซเดียมไอออนเสมือนโซลิดสเตตประสิทธิภาพสูง
[1] วัง WL, GANG Y, PENG J และคณะ ผลของการขจัดน้ำในแคโทดสีน้ำเงินปรัสเซียนสำหรับแบตเตอรี่โซเดียมไอออน โฆษณา ฟังก์ชั่น แม่, 2022, 32(25): 2111727.
[2] MENG XY, LIU YZ, WANG ZY และคณะ เซลล์แบบชาร์จไฟได้กึ่งโซลิดสเตตที่มีพลังงานสูงและความปลอดภัยที่เหนือกว่า เกิดขึ้นได้จากเคมีรีดอกซ์ที่เสถียรของ Li2S ในอิเล็กโทรไลต์แบบเจล สิ่งแวดล้อมด้านพลังงาน วิทย์, 2021, 14(4): 2278.
[3] CHE HY, CHEN SL, XIE YY และคณะ กลยุทธ์การออกแบบอิเล็กโทรไลต์และความคืบหน้าการวิจัยสำหรับแบตเตอรี่โซเดียมไอออนที่อุณหภูมิห้อง สิ่งแวดล้อมด้านพลังงาน วิทย์, 2017, 10(5): 1075.
[4] LI WK, ZHAO N, BI ZJ, และคณะ อิเล็กโทรไลต์เซรามิก Na3Zr2Si2PO12 สำหรับแบตเตอรี่ Na-ion: การเตรียมโดยใช้วิธีการทำแห้งแบบพ่นฝอยและคุณสมบัติของแบตเตอรี่ เจ. อินอร์ก. เม. 2565, 37(2) : 189.
[5] LI D, LEI C, LAI H และคณะ ความก้าวหน้าล่าสุดในอินเทอร์เฟซระหว่างอิเล็กโทรไลต์โซลิดแคโทดและโกเมนสำหรับแบตเตอรี่ลิเธียมไอออนโซลิดสเตตทั้งหมด เจ. อินอร์ก. เม. 2019, 34(7): 694.
[6] KIM KJ, BALAISH M, WADAGUCHI M, และคณะ แบตเตอรี่ Li-metal โซลิดสเตต: ความท้าทายและขอบเขตของอิเล็กโทรไลต์แข็งออกไซด์และซัลไฟด์และส่วนต่อประสาน โฆษณา วัสดุพลังงาน 2021 11(1): 2002689.
[7] GAO H, GUO B, SONG J และคณะ อิเล็กโทรไลต์เจล-โพลีเมอร์/ใยแก้วคอมโพสิตสำหรับแบตเตอรี่โซเดียมไอออน โฆษณา พลังงาน Mater., 2015, 5(9): 1402235.
[8] หลิว YZ, MENG XY, SHI Y และคณะ แบตเตอรี่ไร้แอโนดกึ่งโซลิดสเตตที่มีอายุการใช้งานยาวนาน ใช้งานโดยวิศวกรรมอินเทอร์เฟซควบคู่กับการชดเชย Li โฆษณา แม่, 2023, 35(42): e2305386.
[9] DU GY, TAO ML, LI J, และคณะ แบตเตอรี่โซเดียมไอออนโซลิดสเตตที่มีอุณหภูมิต่ำ อัตราสูงและทนทาน ผลิตจากอิเล็กโทรไลต์โพลีเมอร์และแคโทดสีน้ำเงินปรัสเซียน โฆษณา วัสดุพลังงาน 2020 10(5): 1903351.
(10) PENG J, ZHANG W, LIU QN และคณะ แอนะล็อกสีน้ำเงินปรัสเซียนสำหรับแบตเตอรี่โซเดียมไอออน: อดีต ปัจจุบัน และอนาคต โฆษณา แม่, 2022, 34(15): 2108384.
(11) LU YH, WANG L, CHENG JG และคณะ ปรัสเซียนบลู: โครงสร้างใหม่ของวัสดุอิเล็กโทรดสำหรับแบตเตอรี่โซเดียม เคมี. ชุมชน, 2012, 48(52): 6544.
(12) SÅNGELAND C, Mogensen R, BRANDELL D, และคณะ การหมุนเวียนที่เสถียรของแบตเตอรี่โซลิดสเตตโลหะโซเดียมทั้งหมดพร้อมอิเล็กโทรไลต์โพลีเมอร์ที่ทำจากโพลีคาร์บอเนต แอพพลิเคชัน ACS โพลี เม. 2019, 1(4): 825.
(13) KIM T, AHN SH, SONG YY และคณะ โซเดียมไอออนสีน้ำเงินชนิดปรัสเซียนนำไฟฟ้าอิเล็กโทรไลต์แข็งสำหรับแบตเตอรี่โซลิดสเตตทั้งหมด อังเกว. เคมี. นานาชาติ เอ็ด., 2023, 62(42): e202309852.
(14) ซอง เจ วัง แอล ลู่ ยฮ และคณะ การกำจัด H2O คั่นระหว่างหน้าในเฮกซาไซยาโนเมทัลเลตสำหรับแคโทดที่เหนือกว่าของแบตเตอรี่โซเดียมไอออน เจ.แอม เคมี. สค. 2015 137(7): 2658.
(15) หลิว Y, FAN S, GAO Y และคณะ การสังเคราะห์เชิงโครงสร้างของสารอะนาล็อกสีน้ำเงินปรัสเซียนที่มีธาตุเหล็กสำหรับแบตเตอรี่โซเดียมไอออน เล็ก, 2023, 19(43): e2302687.
(16) วัง W, GANG Y, HU Z และคณะ วิวัฒนาการโครงสร้างแบบพลิกกลับได้ของสีน้ำเงินปรัสเซียนรูปสี่เหลี่ยมขนมเปียกปูนที่อุดมด้วยโซเดียมสำหรับแบตเตอรี่โซเดียมไอออน แนท. คอมมูนิตี้, 2020, 11: 980.
[17] คุณ Y, YU XQ, YIN YX และคณะ โซเดียมเหล็กเฮกซะไซยาโนเฟอร์เรตที่มีปริมาณ Na สูงเป็นวัสดุแคโทดที่มี Na-rich สำหรับแบตเตอรี่ Na-ion นาโนเรส., 2014, 8(1): 117.
(18) REN WH, QIN MS, ZHU ZX, และคณะ การเปิดใช้งานไซต์จัดเก็บโซเดียมในแอนะล็อกสีน้ำเงินปรัสเซียนผ่านการกัดพื้นผิว นาโน เลตต์. 2017, 17(8): 4713.
(19) ZHANG H, GAO Y, PENG J และคณะ แอนะล็อกสีน้ำเงินปรัสเซียนที่มีการวางแนวระนาบคริสตัลที่เหมาะสมที่สุดและมีข้อบกพร่องของคริสตัลต่ำต่อแบตเตอรี่อัลคาไลไอออน 450 Wh·kg−1 อังเกว. เคมี. นานาชาติ เอ็ด., 2023, 62(27): e202303953.
(20) ZHANG ZH, AVDEEV M, CHEN HC และคณะ อะนาล็อกสีน้ำเงินปรัสเซียนลิเธียมเป็นวัสดุแอคทีฟอิเล็กโทรดบวกสำหรับแบตเตอรี่ลิเธียมไอออนที่ไม่มีน้ำเสถียร แนท. ชุมชน, 2022, 13: 7790.
(21) JIANG M, HOU Z, MA H และคณะ การแก้ปัญหาการปิดใช้งานไซต์ Fe หมุนต่ำโดยการกระจายความหนาแน่นของอิเล็กตรอนไปยังแหล่งกักเก็บโซเดียมที่มีพลังงานสูง นาโน เลตต์., 2023, 23(22): 10423.
(22) TANG Z, ZHANG R, WANG HY และคณะ เผยการก่อตัวของรูพรุนแบบปิดของคาร์บอนแข็งที่ได้มาจากเศษไม้สำหรับแบตเตอรี่โซเดียมไอออนขั้นสูง แนท. ชุมชน 2023, 14: 6024.
(23) NIU YB, GUO YJ, หยิน YX และคณะ การชดเชยโซเดียมแคโทดประสิทธิภาพสูงสำหรับแบตเตอรี่โซเดียมไอออน โฆษณา เม. 2020, 32(33): e2001419.





